
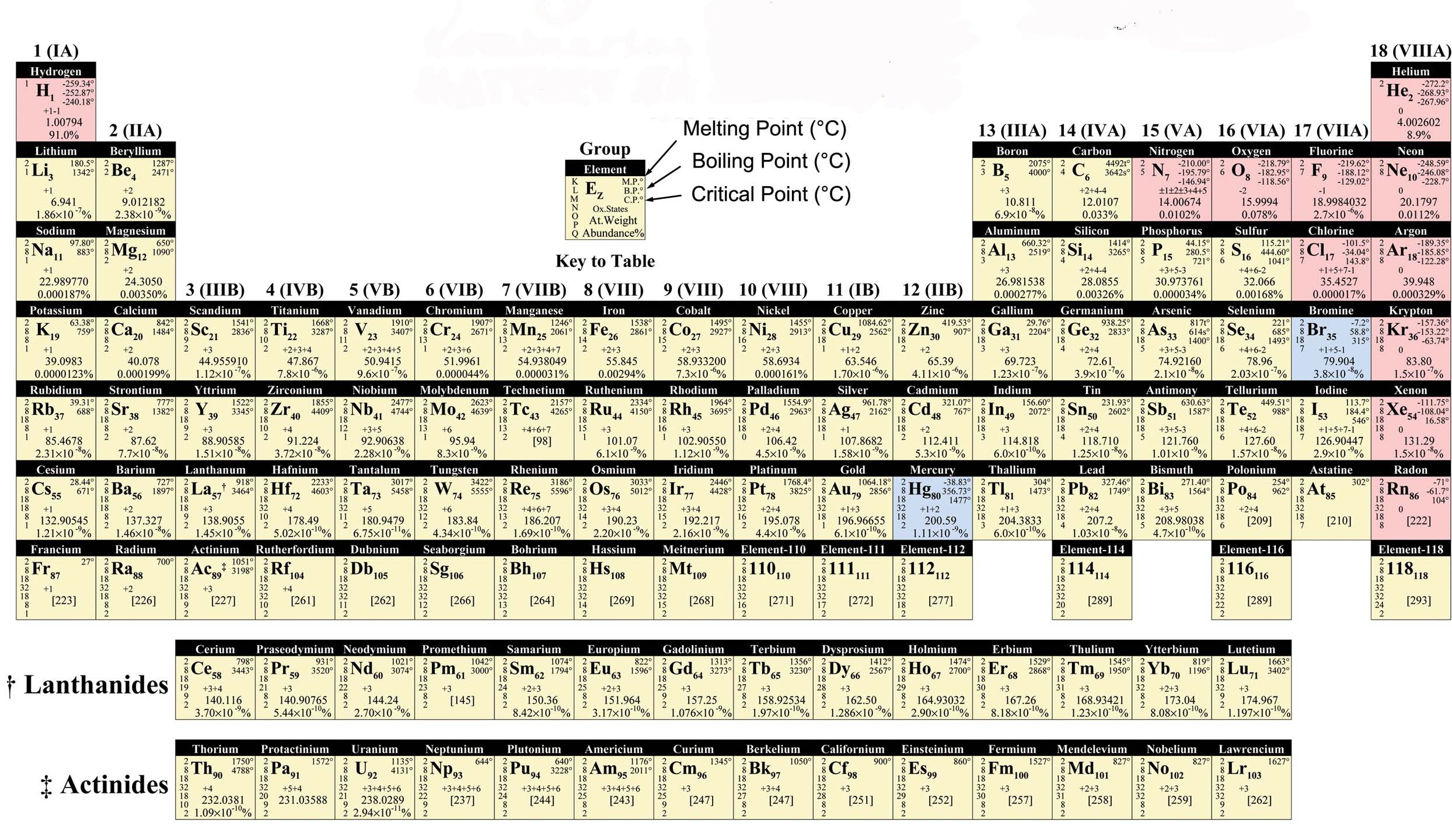
Սա Դ. Ի. Մենդելեևի աղյուսակն է: Այստեղ ամեն տարր ունի իր կարգաթիվը, հարաբերական ատոմային զանգվածը, նշանը, խումբը, պարբերությունը: Օրինակ՝ կալիումի կարգաթիվն է 19: Սա նշանակում է, որ այն ունի տասնինը հատ էլեկտրոն(կայուն վիճակում) և նույնքան էլ պրոտոն: Ar-ը՝(հարաբերական ատոմային զանգված) 39 է: Սա նշանակում է, որ նրա զանգվածի հարաբերությունը ածխածնի զանգվածի 1/12-ին հավասար է 39:Այն գտնվում է չորրորդ պարբերությունում՝ ունի չորս օրբիտալ: Գտնվում է IA(առաջինի ա) խմբում՝ ունի 1 էլեկտրոն արտաքին էներգիական մակարդակում՝ օրբիտալում:Այսպիսով՝ նրա կառուցվածքը այսպիսին է՝
Որպեսզի որոշենք, թե միջուկում քանի նեյտրոն կա, պետք է *Ar-ից հանենք կարգաթիվը:
Մոլ
Մոլը նյութի քանակի չափման միավորն է: Մեկ մոլ նյութը պարունակում է 6,02*10^23 մոլեկուլ: Մեկ մոլ նյութի զանգվածը հավասար է հարաբերական մոլեկուլային զանգվածին(Mr), որն էլ հավասար է նյութի կազմի մեջ մտնող բոլոր ատոմների Ar-երի գումարին: Պետք է հաշվի առնել նաև այն, թե մոլեկուլում քանի հատ կա տվյալ ատոմից: Մոլը նշանակում են n տառով: n=N/NԱ որտեղ N-ը մոլեկուլների քանակն է, իսկ NԱ-ն՝ **Ավոգադրոյի հաստատունը:Կա նաև այսպիսի բանաձև՝ n=m/M, որտեղ m-ը նյութի զանգվածն է(գրամներով), իսկ M-ը ՝ թվապես հավասար է Mr-ին բայց սրա չափման միավորն է գրամ/մոլ: Սրանից կարելի է դուրս բերել նաև հետևյալ բանաձևերը՝ m=n*m և M=m/n:
Քիմիական ռեակցիաներ

Քիմիական ռեակցիաները լինում են չորս տեսակի՝
- Միավորման-Երբ երկու նյութից առաջանում է մեկ այլ նյութ: Օրինակ՝ 2H2 + O2 = 2H2O
- Քայքայման-Երբ մեկ նյութից առաջանում են երկեւ այլ նյութեր: Օրինակ՝ H2SO4 = H2O + SO3
- Տեղակալման- Երբ մեկ բարդ և մեկ պարզ նյութից առաջանում են երկու այլ նյութ: Օրինակ՝ CH4 + Cl2 = CH3Cl + HCl
- Իոնափոխանակման- Երբ երկու բարդ նյութերից առաջանում են այլ բարդ նյութեր: Օրինակ՝ H2SO4 + 2NaCl = 2HCl + Na2SO4
*Ar-հարաբերական ատոմային զանգված:
**Ավոգադրոյի հաստատուն-6.02*10^23
